上一篇:曼恒數(shù)字發(fā)力3D打印領(lǐng)域,成為MakerBot中國區(qū)獨(dú)家總代 下一篇:中國鑫達(dá)在哈爾濱7億投建3D打印耗材智能制造示范工廠 | |
相關(guān)帖子
|
|

ORNL開發(fā)3D打印智能追蹤器包裝,,增強(qiáng)放射性
3D People 推出PartsVault云平臺(tái),,軟件驅(qū)動(dòng)

金屬 3D 打印助力百年老摩托車重?zé)ㄉ鷻C(jī)

美國3D打印上市公司股價(jià)繼續(xù)下跌,特朗普高

維爾紐斯大學(xué)發(fā)布開創(chuàng)性多光子3D光刻技術(shù)指

海外3D打印概念股ETF-ARK市值只有5300多萬

報(bào)名:助力中國3D打印企業(yè)出�,;顒�(dòng)首站——

報(bào)名:2025增材制造前沿技術(shù)突破與產(chǎn)業(yè)協(xié)同

杰普特2024年?duì)I收14.57 億元,,3D打印激光器
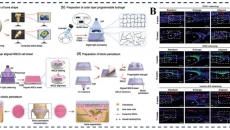
3D 打印遇上血管化骨修復(fù):搭建骨骼健康的

關(guān)注南極熊

通知
聯(lián)系QQ/微信9:00-16:00
392908259南極熊3D打印網(wǎng)
致力于推動(dòng)3D打印產(chǎn)業(yè)發(fā)展