神經(jīng)干細(xì)胞(NSCs)移植可以實(shí)現(xiàn)部分神經(jīng)回路和功能的重建,是脊髓損傷(SCI)一種極具前景的治療方式。然而直接移植到病變部位的NSCs存活率低,分化易失控。3D生物打印可以構(gòu)建NSCs分布均勻且具有精確而又復(fù)雜的脊髓樣結(jié)構(gòu)的載細(xì)胞支架,有望為NCSs提供了合適的微環(huán)境并促進(jìn)病變區(qū)域的細(xì)胞-支架和細(xì)胞-細(xì)胞相互作用,這對外源性NSCs在體內(nèi)進(jìn)行神經(jīng)元再生和軸突連接意義重大。
近期,中科院蘇州納米技術(shù)與納米仿生研究所的張智軍教授團(tuán)隊(duì)開發(fā)了一種可用于制造載NSCs神經(jīng)組織支架的3D生物打印策略。打印的支架能為NSCs的生長和神經(jīng)分化提供良好的微環(huán)境、促進(jìn)軸突再生、減少膠質(zhì)疤痕形成以及優(yōu)化神經(jīng)網(wǎng)絡(luò)的形成,最終能幫助恢復(fù)SCI模型大鼠的運(yùn)動能力,實(shí)現(xiàn)SCI修復(fù)。相關(guān)成果 “3D bioprinted neural tissue constructs for spinal cord injury repair”發(fā)表于Biomaterials上。

640.jpg (157.37 KB, 下載次數(shù): 188)
下載附件
2024-4-16 09:36 上傳
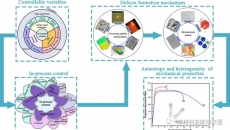
圖1 HBC/HA/MA生物墨水3D打印前后的交聯(lián)反應(yīng)以及載NSCs神經(jīng)組織支架的3D生物打印示意圖
生物墨水組成:羥丙基殼聚糖(HBC)、巰基化透明質(zhì)酸(HA-SH)、乙烯砜化透明質(zhì)酸(HA-VS)和基質(zhì)膠(matrigel ,MA)
工藝:HBC/HA-SH/MA與HA-VS溶液冰浴混勻后得到HBC/HA/MA-0.3生物墨水(HBC 3% w/v, HA-SH0.3% w/v, HA-VS 0.3% w/v, MA 0.1% w/v) 或者BC/HA/MA-0.6生物墨水(HBC 3% w/v, HA-SH0.6% w/v, HA-VS 0.6% w/v, MA 0.1% w/v)。將HBC/HA/MA生物墨水置于37℃放置2h,即交聯(lián)形成HBC/HA/MA水凝膠;NSCs與HBC/HA/MA生物墨水混合冰浴5min則可獲得載細(xì)胞的生物墨水。
3D生物打印條件:擠出式生物3D打印法;注射器溫度10℃,打印平臺溫度37℃,打印壓力約20 kPa
1. HBC/HA/MA生物墨水的表征
1)剪切變稀特性、凝膠速度以及機(jī)械強(qiáng)度表征
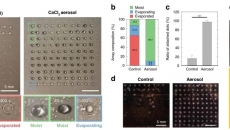
HBC/HA/MA生物墨水具有典型的剪切稀釋行為。它在低溫下具有很好的流動性,升溫至37℃后則能迅速交聯(lián)成水凝膠。通過對比HBC和 HBC/HA/MA的凝膠時(shí)間(彈性模量G '=損耗模量G "時(shí)的時(shí)間),發(fā)現(xiàn)同濃度的HBC與HBC/HA/MA生物墨水具有相似的凝膠時(shí)間,這說明HBC在HBC/HA/MA生物墨水的快速凝膠化中起主要作用。此外,HBC/HA/MA水凝膠的機(jī)械強(qiáng)度明顯高于HBC以及無化學(xué)鍵合的HBC/HA/MA水凝膠,且其機(jī)械強(qiáng)度在一定范圍內(nèi)與HA濃度呈正比(圖2)。
2)溶脹率、穩(wěn)定性以及形態(tài)結(jié)構(gòu)表征
研究人員用掃描電子顯微鏡(SEM)觀察了HBC/HA/MA水凝膠的形態(tài)結(jié)構(gòu),發(fā)現(xiàn)水凝膠內(nèi)部為尺寸較均勻(約100 μm)的高孔結(jié)構(gòu),而孔隙尺寸在一定范圍內(nèi)會與HA濃度呈反比。他們還通過溶脹比分析以及體外降解試驗(yàn)觀察了HBC/HA/MA水凝膠的溶脹率和降解行為。發(fā)現(xiàn)HBC/HA/MA水凝膠溶脹率低于HBC水凝膠,但其與細(xì)胞培養(yǎng)相關(guān)的平衡含水率未受顯著影響。此外,交聯(lián)度高的水凝膠穩(wěn)定性高,不易降解(圖2)。

640-1.jpg (145.24 KB, 下載次數(shù): 207)
下載附件
2024-4-16 09:36 上傳
圖2 HBC/HA/MA生物墨水的相關(guān)表征
2. 載NSCs的3D打印HBC/HA/MA支架的制備與相關(guān)檢測
研究者用含NSCs的HBC/HA/MA生物墨水制備了方形網(wǎng)格支架(打印過程中支架微觀結(jié)構(gòu)未見變形或坍塌)并用Live/Dead assay評估了支架中NSCs的活力,發(fā)現(xiàn)其細(xì)胞活力與增殖能力較高。SEM結(jié)果也顯示,粘附在支架上的NSCs在培養(yǎng)7 d后充分延伸,形成了富含絲狀偽足的細(xì)胞間連接。他們還通過免疫熒光染色研究了生物打印后NSCs的分化能力:發(fā)現(xiàn)支架中的細(xì)胞表達(dá)星形膠質(zhì)細(xì)胞標(biāo)記物GFAP、神經(jīng)元特異性細(xì)胞骨架蛋白Tuj1,并能成功分化為成熟神經(jīng)元;他們還發(fā)現(xiàn)支架中HA的濃度對NSCs的神經(jīng)元分化有重要影響,HBC/HA/MA-0.3支架中的NSCs具有較高的分化率(圖3)。

640-2.jpg (238.82 KB, 下載次數(shù): 193)
下載附件
2024-4-16 09:36 上傳
圖3 載NSCs的HBC/HA/MA支架的相關(guān)檢測
3. 3D打印的載NSCs的線性陣列樣支架用于SCI大鼠治療
1)運(yùn)動功能評估
研究者打印了模擬天然脊髓白質(zhì)結(jié)構(gòu)的載NSCs線性陣列樣支架(后面統(tǒng)稱:載NSCs支架),然后將支架移植于T8-9脊髓完全橫斷的脊髓損傷模型大鼠的脊髓橫斷處。最后通過Basso-Beattie-Bresnahan (BBB)試驗(yàn)以及柔性壓力傳感器實(shí)時(shí)監(jiān)測手段,對載NSCs支架(治療劑量:3×105)移植、空支架移植以及未治療組大鼠的后肢肌肉和關(guān)節(jié)的運(yùn)動情況進(jìn)行了評估。發(fā)現(xiàn)相較于后肢未見明顯運(yùn)動的對照組大鼠。植入了載NSCs支架的大鼠的運(yùn)動功能明顯恢復(fù),且同時(shí)出現(xiàn)了臀部和膝蓋踝關(guān)節(jié)運(yùn)動。載NSCs支架移植組修復(fù)SCI的效果優(yōu)于空支架移植組和對照組(圖4A-E)。
2)組織學(xué)分析
為了進(jìn)一步研究載NSCs支架對SCI的治療效果,研究者對植入支架12周后的各組小鼠的損傷脊髓進(jìn)行了組織學(xué)分析,通過免疫熒光染色檢測神經(jīng)元、軸突以及少突膠質(zhì)細(xì)胞的再生,并研究了脊髓損傷區(qū)神經(jīng)纖維生長和髓鞘形成的情況。發(fā)現(xiàn):載NSCs支架移植組病變區(qū)可見明顯Tuj1、NF、Oligo2、GAP-43、以及髓鞘堿性蛋白(MBP)的陽性染色,而GFPA表達(dá)則較低。這表明載NSCs支架促進(jìn)了損傷部位軸突和髓鞘形成、神經(jīng)元的分化并抑制了膠質(zhì)瘢痕的形成(圖4F)。
3)植入后NSCs的存活及分化
研究者制備了載GFP-NSCs支架并將其植入病損區(qū)。然后在移植12周后取樣進(jìn)行免疫熒光染色來監(jiān)測外源性NSCs在體內(nèi)的命運(yùn)。結(jié)果顯示隨支架移植的NSCs能存活至少12周,且GFP與大部分的Tuj1、NF、Oligo2定位一致,這提示存活的NSCs分化為了Tuj1陽性的神經(jīng)元以及Oligo2陽性的少突膠質(zhì)細(xì)胞。而未與GFP抗體共染的神經(jīng)元和少突膠質(zhì)細(xì)胞的存在則提示可能有內(nèi)源性NSCs遷移至損傷區(qū)域參與損傷修復(fù)。這些結(jié)果均表明載NSCs的支架為NSCs提供了良好的微環(huán)境(圖4G-H)。

640 2.jpg (148.18 KB, 下載次數(shù): 194)
下載附件
2024-4-16 09:36 上傳
圖4 載NSCs支架移植促進(jìn)SCI大鼠的脊髓損傷修復(fù)的相關(guān)評估
4. 總結(jié)
HBC/HA/MA水凝膠具有適合NSCs生長的降解速率、孔隙率和機(jī)械強(qiáng)度。利用HBC/HA/MA水凝膠制備的載NSCs支架為NSCs提供了良好的微環(huán)境,支架中的NSCs存活率高,增殖能力強(qiáng),具有良好的神經(jīng)分化能力。載NSCs支架移植后能促進(jìn)脊髓損傷區(qū)的軸突和髓鞘形成,抑制膠質(zhì)瘢痕形成,明顯改善SCI大鼠的運(yùn)動功能。該3D生物打印的載NSCs支架有望應(yīng)用于神經(jīng)組織工程和其他再生醫(yī)學(xué)領(lǐng)域。
文章來源:
https://doi.org/10.1016/j.biomaterials.2021.120771
|